Moderna pidió la aprobación de su vacuna contra COVID-19 en EE.UU y Europa
La compañía informó que solicitó autorización para el uso de la vacuna a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y una autorización parcial a la Agencia Europea del Medicamento (EMA). Dicen que tiene 94,1% de eficacia en los casos severos.
Por Canal26
Lunes 30 de Noviembre de 2020 - 10:28
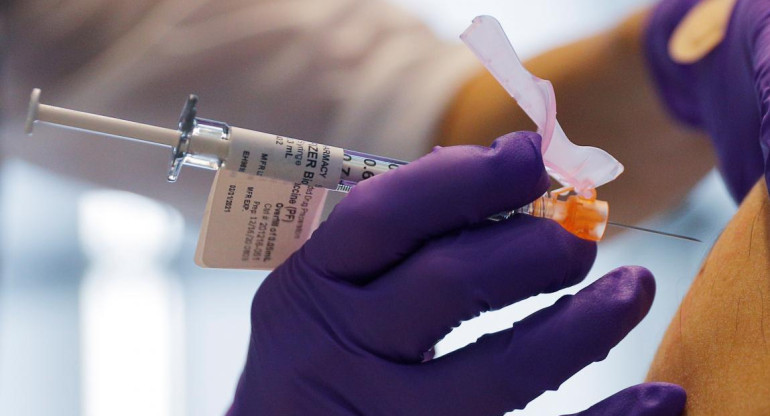
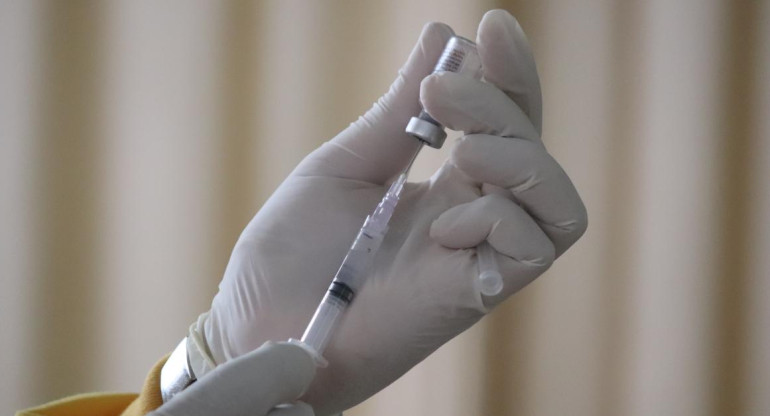
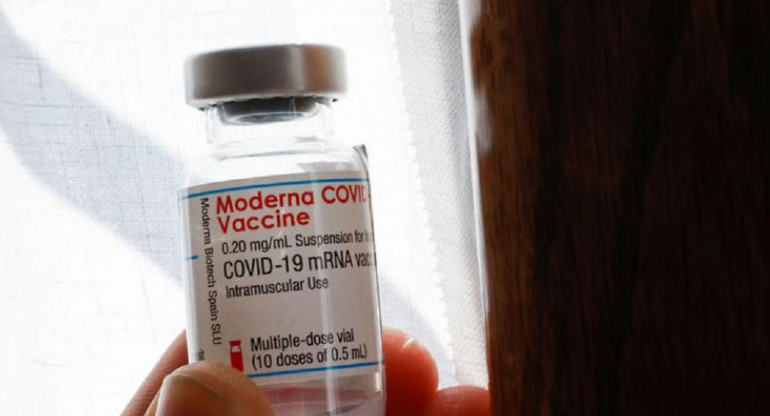
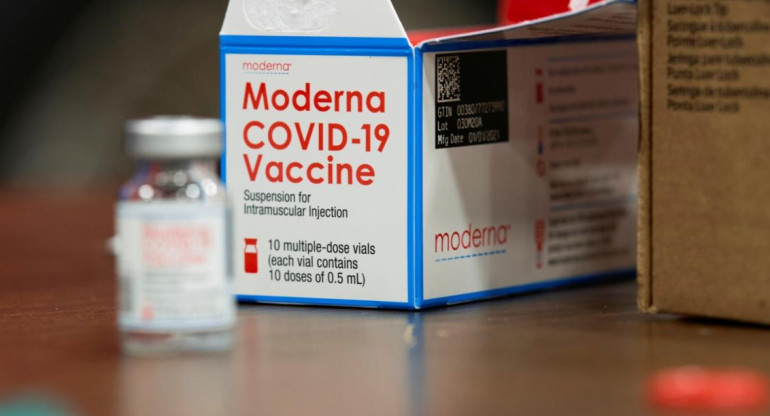
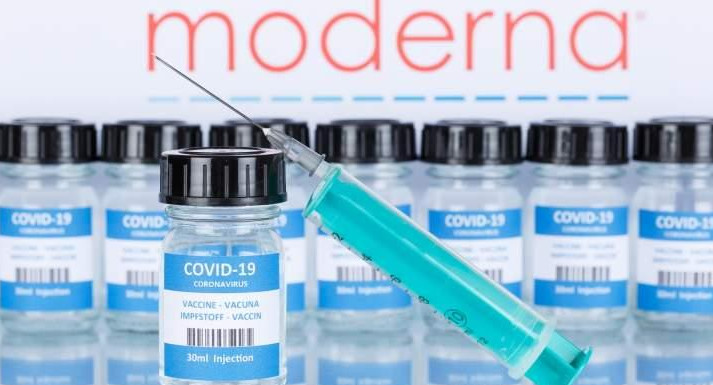
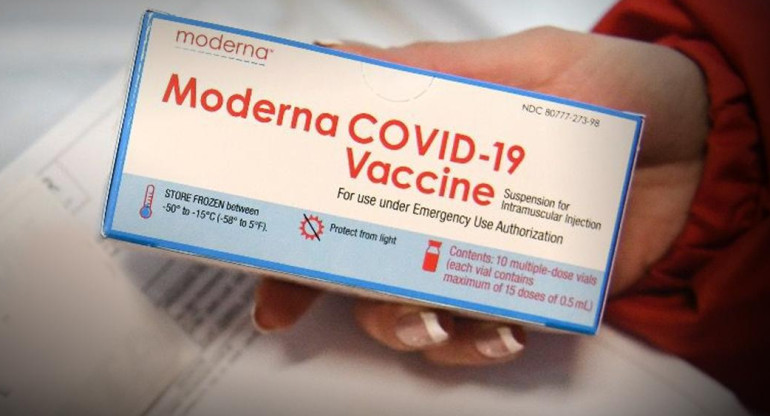
 Moderna pedirá aprobación de su vacuna contra COVID-19 en EE.UU y Europa. REUTERS
Moderna pedirá aprobación de su vacuna contra COVID-19 en EE.UU y Europa. REUTERS
Moderna pedirá la aprobación de su vacuna contra la COVID-19 en EE.UU y Europa. La compañía informó que planean solicitar este lunes 30 de noviembre una autorización para el uso de la vacuna a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y una autorización parcial a la Agencia Europea del Medicamento (EMA).
La empresa dijo que la vacuna tiene 94,1% de eficacia en los casos severos.
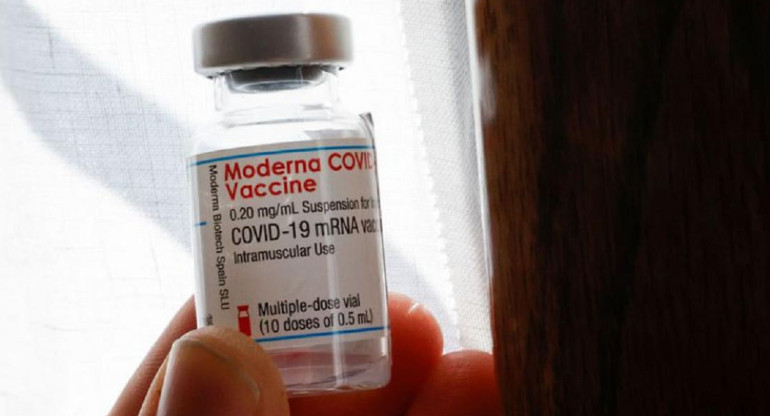
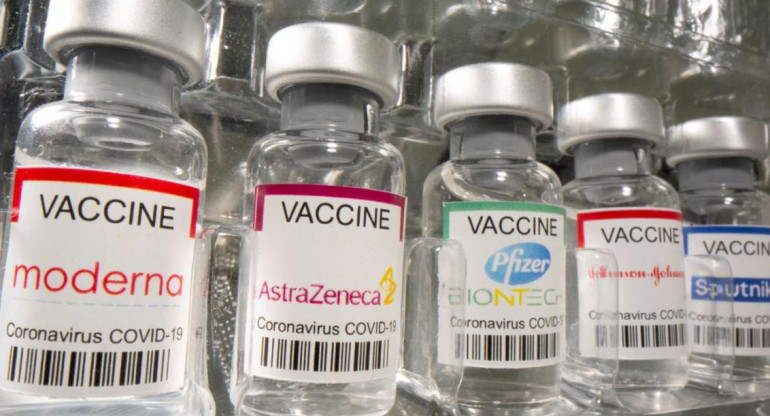
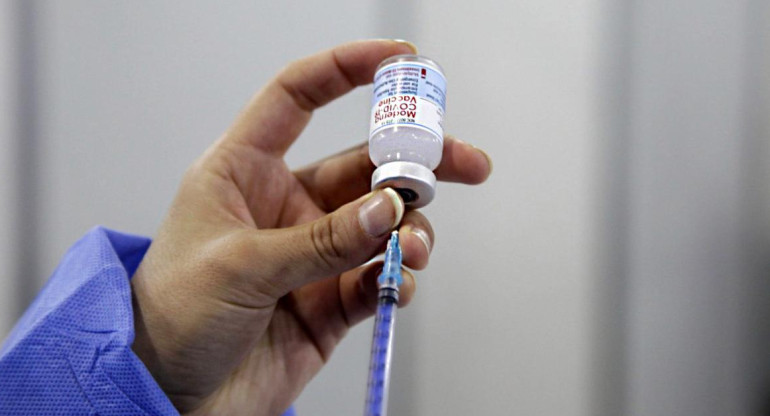
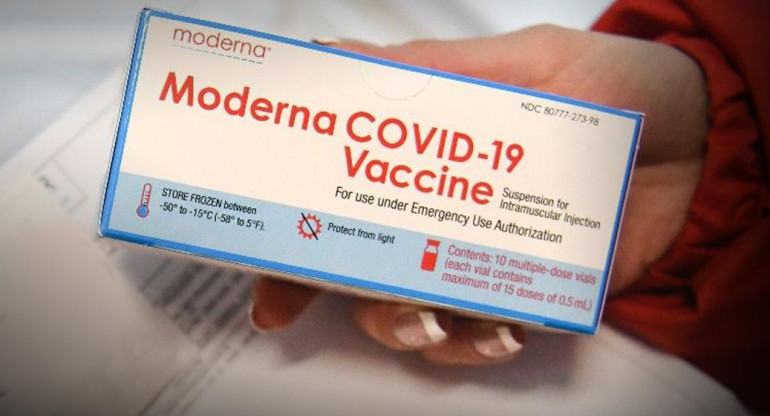
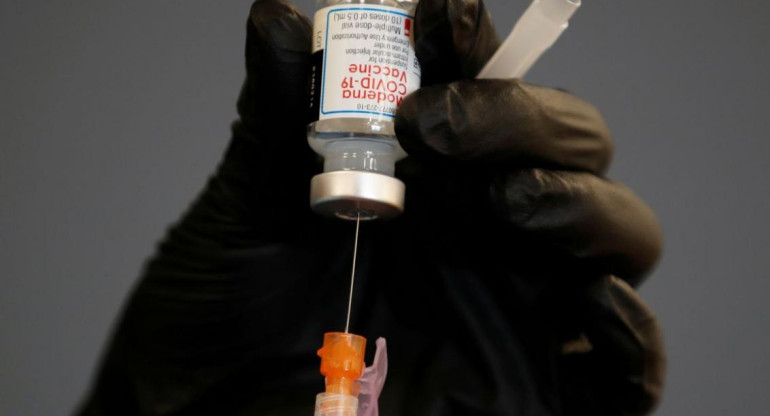
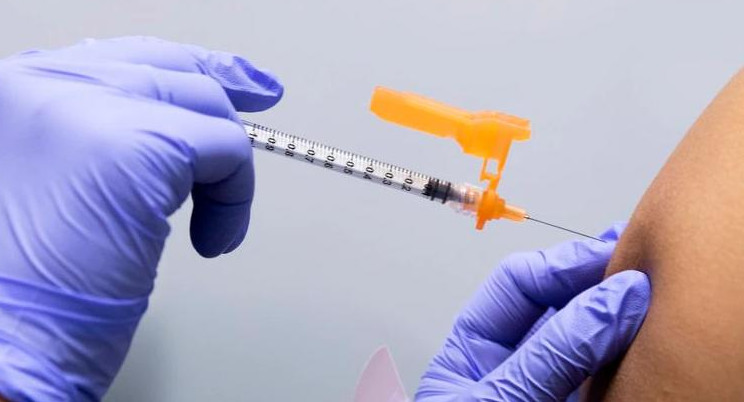
 Moderna. Foto Archivo.
Moderna. Foto Archivo.
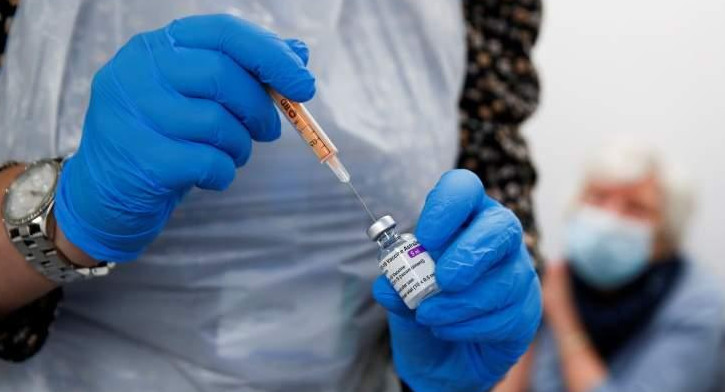
La empresa estadounidense Moderna anunció que presentó este lunes solicitudes de emergencia de autorización para su vacuna contra el covid-19 en Estados Unidos y en Europa, luego de que resultados completos confirmaran una alta eficacia de la misma (94,1%).
Dos semanas después de haber anunciado una eficacia de 94,5% sobre la base de resultados preliminares, Moderna reportó que de 196 participantes en su ensayo clínico que se infectaron con covid-19, 185 pertenecían al grupo placebo y 11 al grupo vacunado, con una eficacia calculada de 94,1%. Ninguna forma grave de la enfermedad se registró en el grupo vacunado.
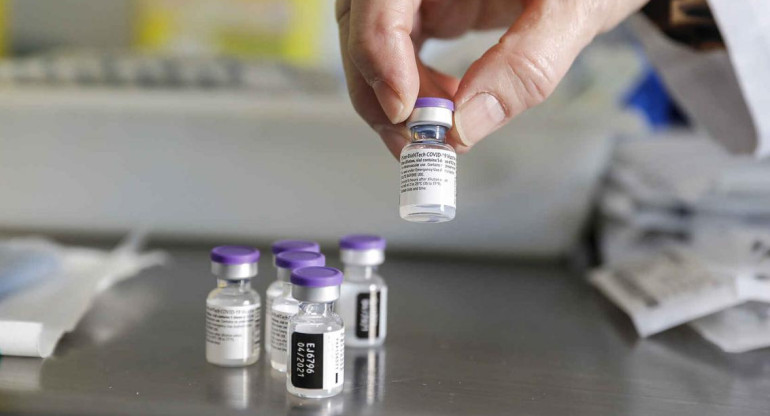
El laboratorio pidió la autorización para comercializar su vacuna contra el coronavirus tanto a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) como a la Agencia Europea del Medicamento. Los reguladores analizarán los datos de prueba de la vacuna de ARNm y decidirán si es lo suficientemente segura y efectiva como para recomendar su implementación.
We just announced the primary efficacy analysis in the Phase 3 COVE study for mRNA-1273, our COVID-19 vaccine candidate and that today, we plan to request an Emergency Use Authorization from the U.S. FDA & conditional approval from the EMA. Read more: https://t.co/90FbcVHdWN pic.twitter.com/36tpY0QeFl
— Moderna (@moderna_tx) November 30, 2020
Temas del momento
Más Leídas
-
1
Un enemigo silencioso: el aparato que hay que desconectar sí o sí en otoño para evitar incendios

-
2
Llega el día más frío del año: recomendaciones y cuidados a tener en cuenta para no sufrir las bajas temperaturas

-
3
PAMI abril 2025: los hospitales y centros de salud exclusivos para los jubilados

-
4
Irlanda ofrece trabajo remoto con salario medio alto: los requisitos para postularse y el monto

-
5
Las clásicas calzas de gimnasio no van más: la nueva tendencia fitness para ir a entrenar en otoño-invierno 2025

Notas relacionadas
También podría interesarte

Volodimir Zelenski denunció que Rusia atacó su ciudad natal con un misil balístico: "No quiere un alto el fuego"

Final explicado de "Atrapados": quién es el verdadero culpable, qué pasó con Leo Mercer y por qué desapareció Martina Schulz

La ANMAT prohibió marca de gomitas con una sustancia química del cannabis: "No se puede garantizar seguridad"

Falkland, el inglés de linaje que asegura que las Malvinas son argentinas y habla de "piratería británica"